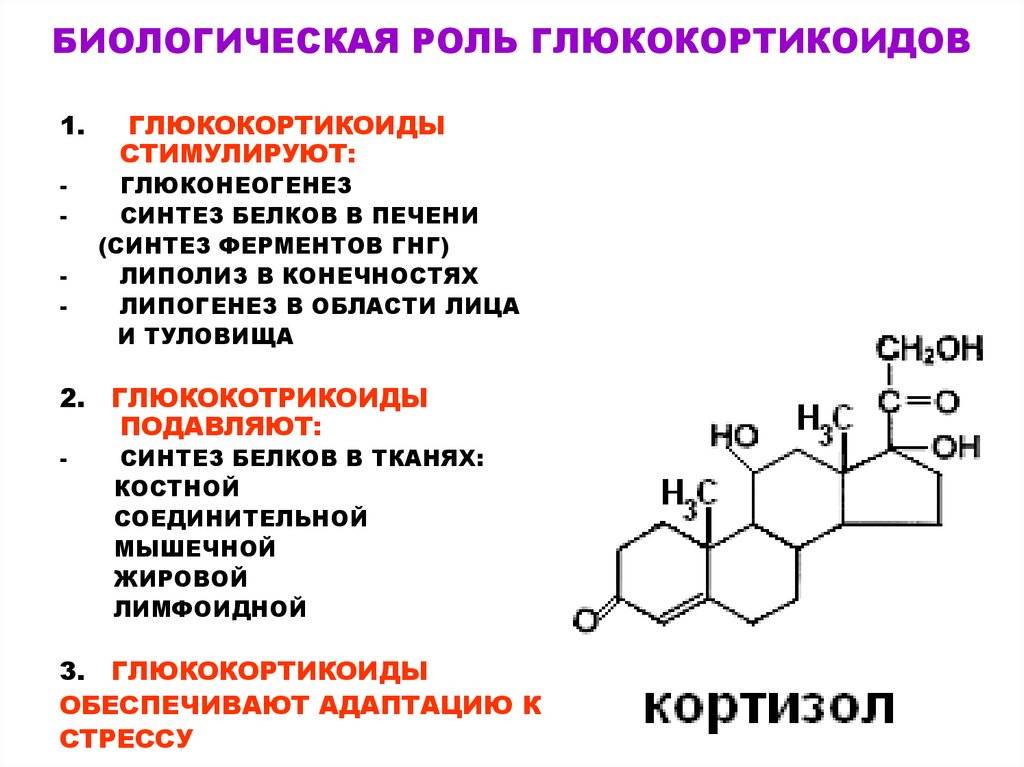
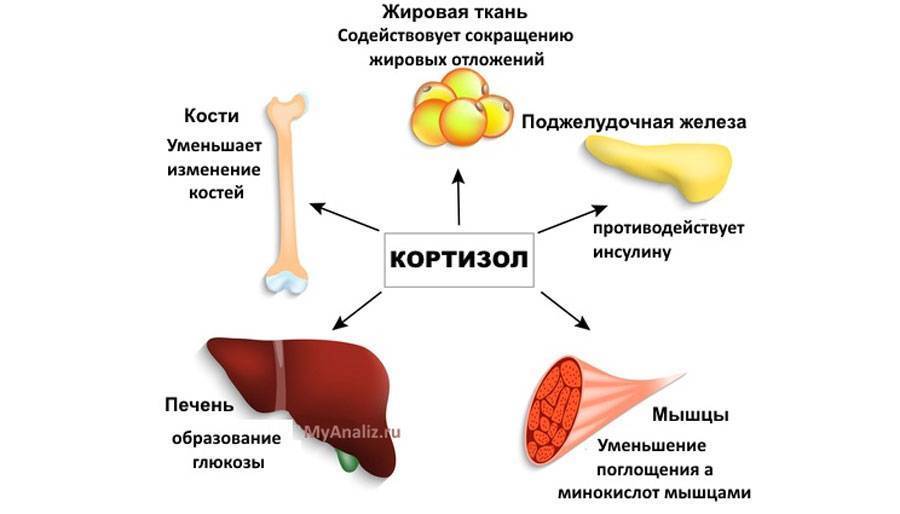
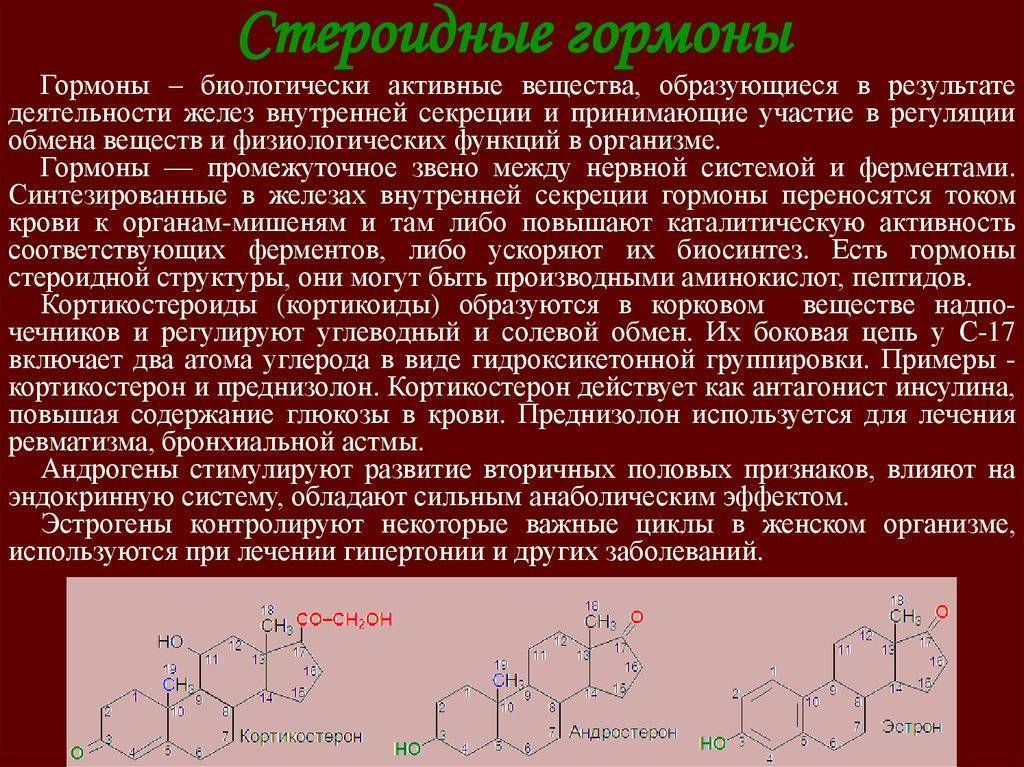
Гормоны коры надпочечников и их функции
В надпочечниках вырабатываются разные гормоны с абсолютно разными функциями. По этому признаку их можно разделить на группы.
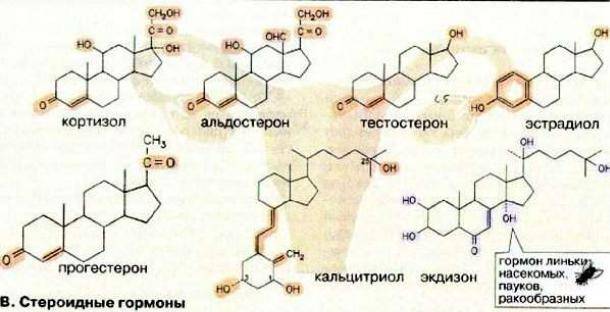
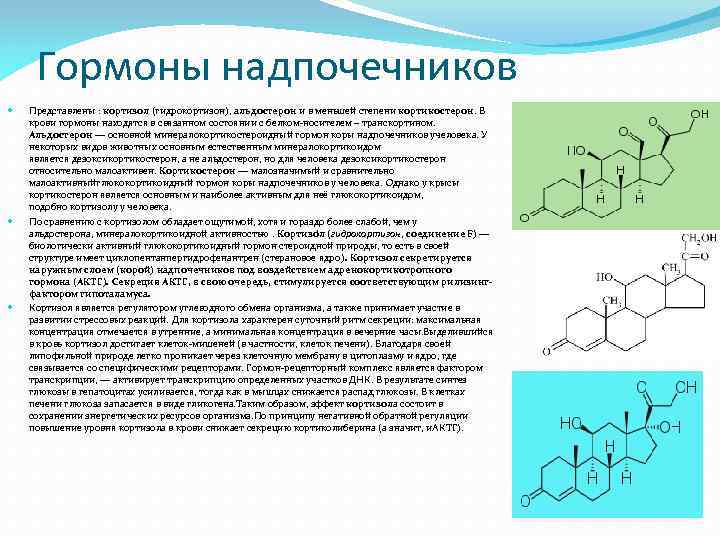
Гормоны, выделяемые корковым отделом надпочечников
Минералокортикоиды
Наиболее сильную активность среди этих гормонов демонстрирует альдостерон – органическое химическое соединение из группы стероидов. Функции альдостерона:
- участвует в регуляции водно-минерального баланса организма, поддерживает надлежащий уровень минеральных солей и воды в организме;
- влияет на функционирование почечных канальцев, увеличивая всасывание солей натрия и ограничивая их экскрецию с мочой;
- уменьшает количество крови, проходящей через почки, тем самым уменьшая количество выделяемой мочи;
- участвует в транспортных процессах в почках;
- вместе с ренином и ангиотензином регулирует кровяное давление.
Глюкокортикостероиды
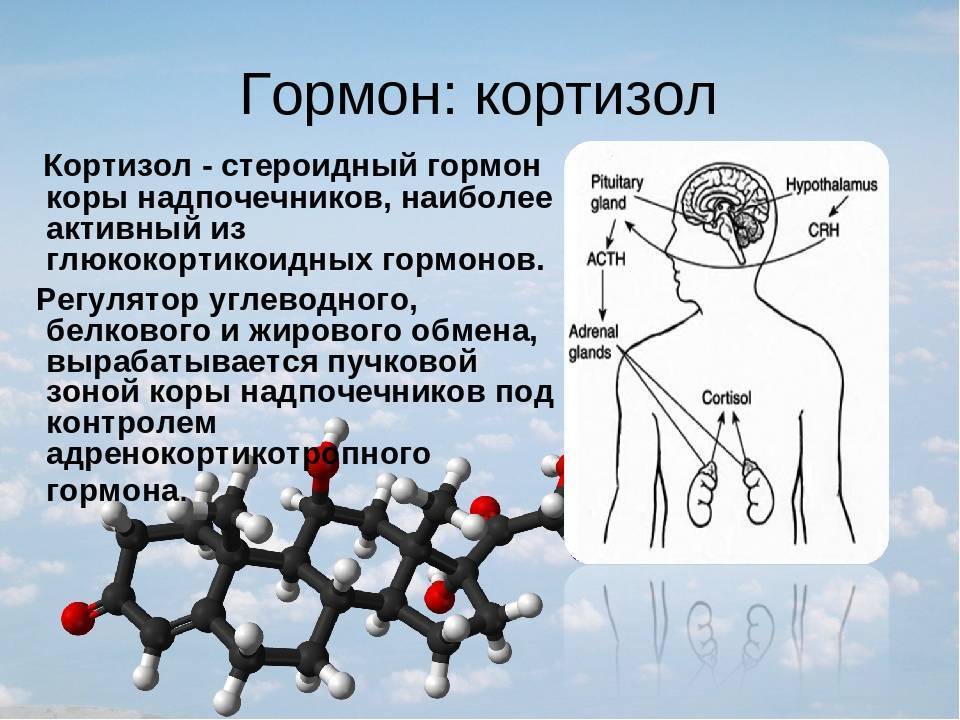
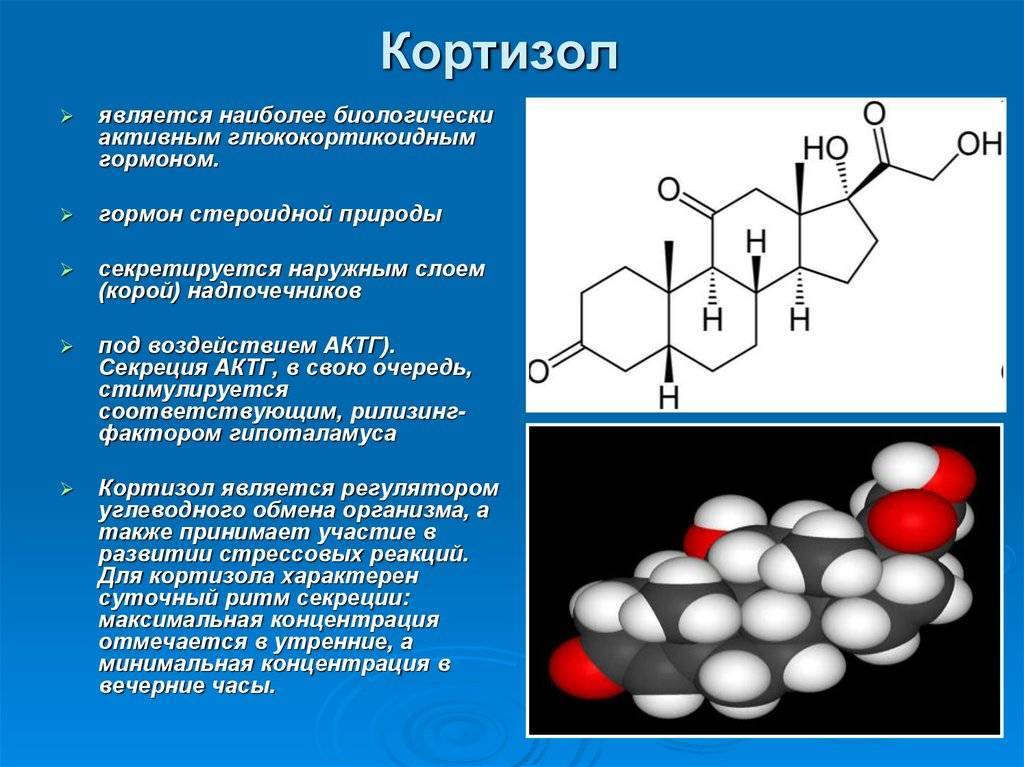
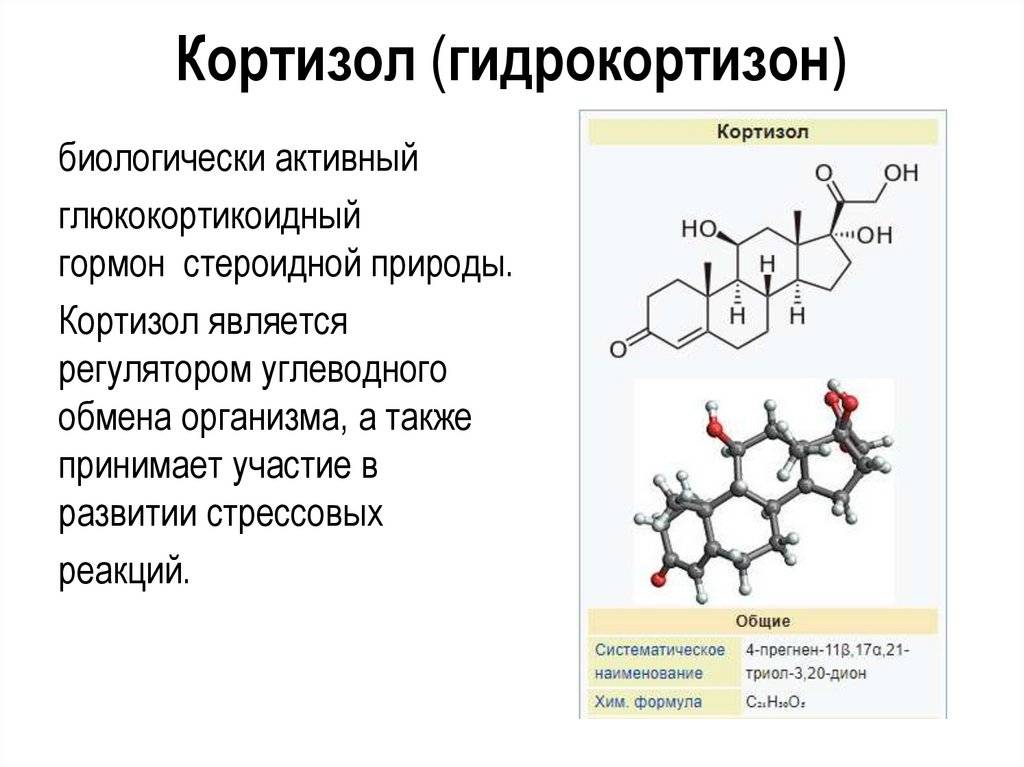
Наиболее важный гормон в группе глюкокортикоидов – кортизол, известный как гормон стресса. Характерная особенность кортизола – циркадный ритм секреции, поэтому наибольшая его концентрация наблюдается в утренние часы, а наименьшая около полуночи.
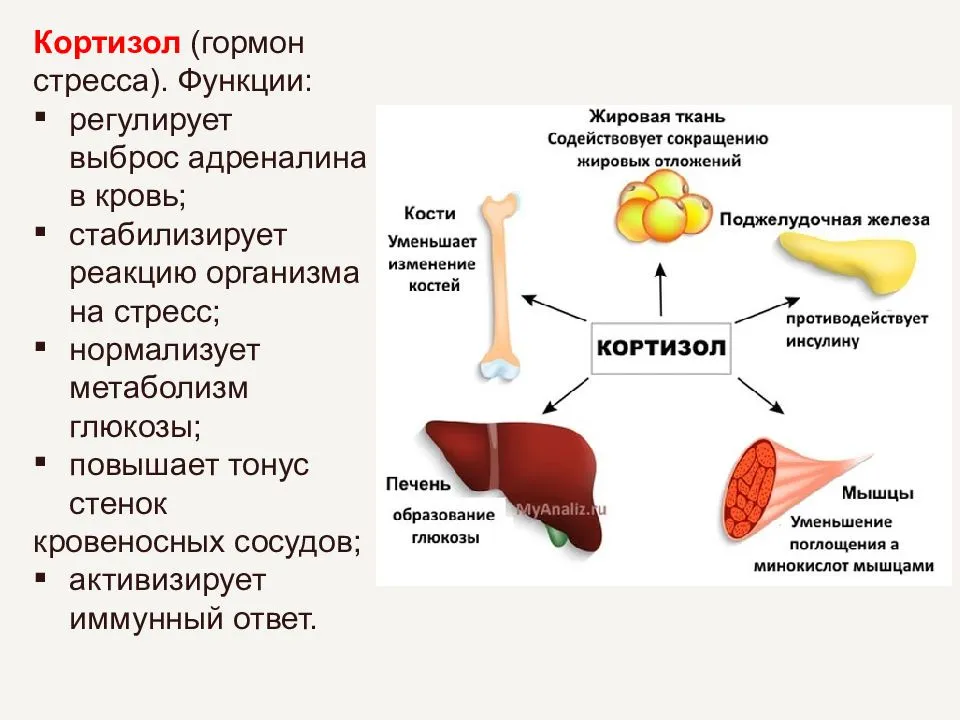
Функции кортизола:
- обладает противовоспалительными свойствами, поэтому часто входит в состав сильнодействующих препаратов для противодействия воспалению;
- влияет на уровень глюкозы в крови, вызывает повышение уровня глюкозы, например, в стрессовые моменты;
- способствует высвобождению аминокислот, ускорению глюконеогенеза – образованию глюкозы из неуглеводных соединений, задержке солей в организме;
- участвует в расщеплении жирных кислот и снижает использование глюкозы скелетными мышцами при интенсивных физических нагрузках.
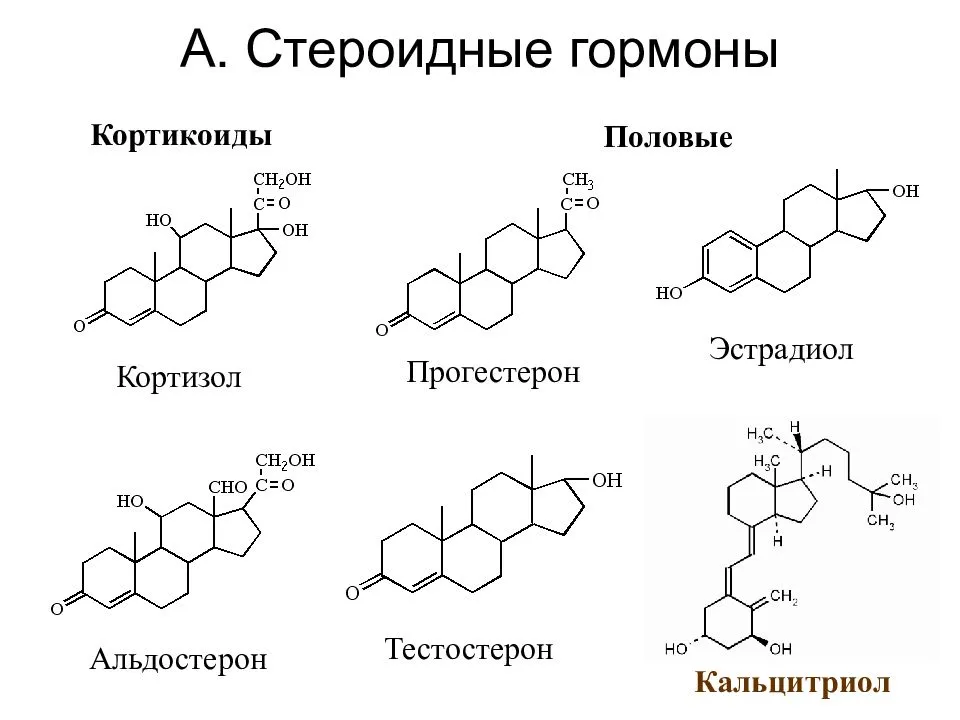
Половые гормоны – андрогены
Андрогены, например, тестостерон, вырабатываются в надпочечниках в небольшом количестве. Эти гормоны ускоряют рост организма и отвечают за формирование вторичных мужских половых признаков.
Гормоны, выделяемые мозговым веществом надпочечников
Адреналин
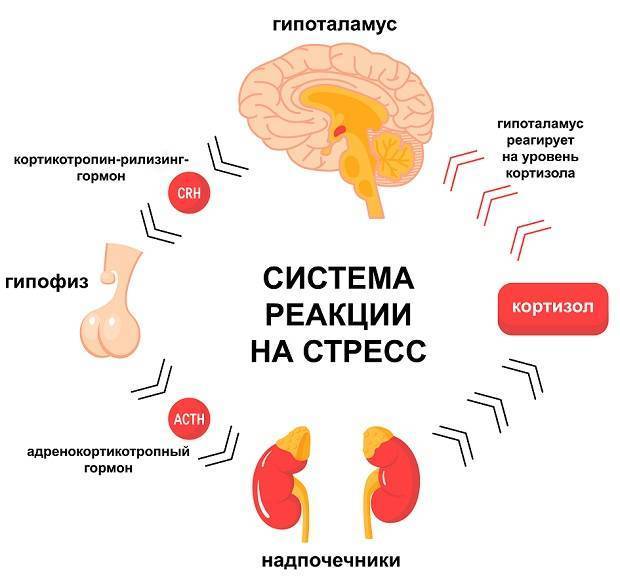
Задача адреналина – повлиять на реакцию организма в ситуации стресса или возникающей опасности. При увеличении уровня адреналина в крови:
- учащается сердцебиение;
- повышается артериальное давление;
- расширяются зрачки;
- угнетается перистальтика кишечника;
- увеличивается уровень глюкозы в крови.
Адреналин вводят больным в случаях анафилактического шока или реанимации.
Норадреналин
Норадреналин вырабатывается не только в мозговом веществе надпочечников, но и в ядрах ствола головного мозга. Функции норадреналина:
- воздействует на систему кровообращения, повышая систолическое и диастолическое артериальное давление;
- действуя на симпатические нервы кишечника, снижает тонус кишечника.
Во время сна выделение норадреналина незначительно, при пробуждении и вставании оно увеличивается;
Дофамин
Дофамин вырабатывается в небольших количествах в мозговом веществе надпочечников, но в основном синтезируется в нейронах. Функции дофамина:
- способствует выработке положительного психоэмоционального настроя, проявлению эмоций;
- регулирует концентрацию других гормонов, особенно пролактина;
- повышает кровяное давление и силу мышечного сокращения – это свойство дофамина используется при лечении травматического, септического и кардиогенного шоков.
Препараты кортизона
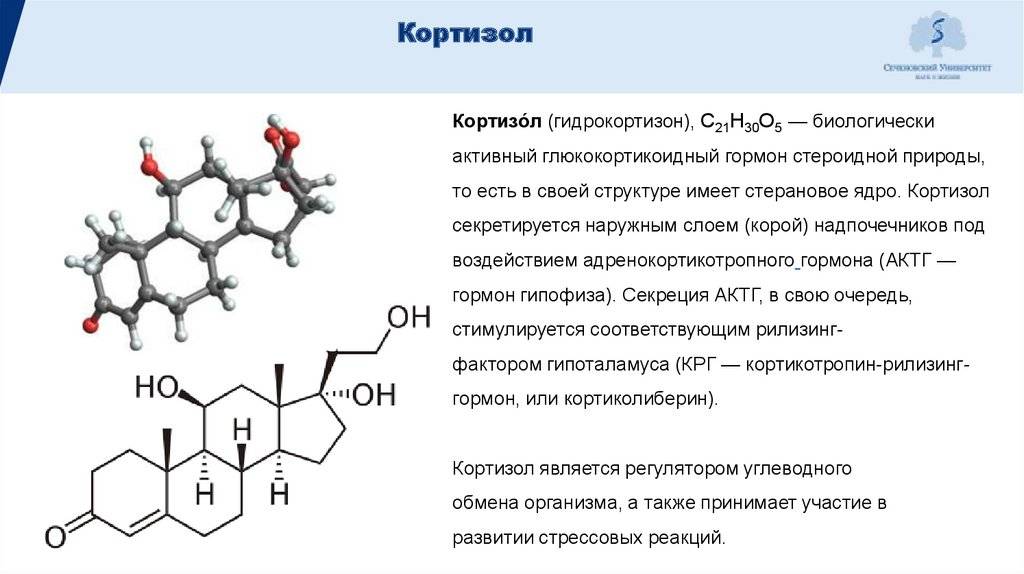
К. был первым кортикостероидом, примененным Ф. Хенчем (1948) в клин, практике. Промышленное получение К. осуществляется из природных стероидных веществ: стеринов (холестерин, эргостерин, стигмастерин), желчных к-т (холевая, дезоксихолевая, тиодезоксихолевая), растительных веществ — сапонинов, а также ортотолуидина, эргостерона (получаемого из дрожжей), прогестерона (получаемого из восточноафриканского вида алоэ).
Для клин, применения выпускается кортизона ацетат (Cortisoni acetas; 11-дегидро-17-оксикортико-стерон ацетат); применяется гл. обр. при состояниях, требующих быстрого терапевтического эффекта: при анафилактическом, послеоперационном и других видах шока, при коллапсе. Эффективен К. при лечении заболеваний соединительной ткани (острой стадии ревматизма, диссеминированной красной волчанки, панартериита и др.). В гематол, практике К. применяют при иммунол. конфликтах (аутоиммунных гемолитических анемиях, тромбоцитопении, иммунном агранулоцитозе). К. является специфическим лимфотропным препаратом, однако при ряде заболеваний предпочтение отдается синтетическим препаратам других глюкокортикоидных гормонов (напр., преднизолону, дексаметазону, триамсинолону), поскольку они, по сравнению с К., реже вызывают побочные действия. При воздействии К. на воспалительные процессы угнетается активность гиалуронидазы, снижается проницаемость капилляров и клеточных мембран, тормозится экссудация и эмиграция лейкоцитов (см. Воспаление); вызывается лизис лимфоцитов и плазматических клеток, что приводит к уменьшению продукции антител и угнетению реакции антиген — антитело. При применении препаратов К. подавляется продукция фибробластов и ретикулярных клеток, а также мобилизуется костномозговой резерв гранулоцитов, в связи с чем наблюдается эозинопения и реактивный нейтрофильный лейкоцитоз (повышается элиминация гранулоцитов из костного мозга).
Дозы К. определяются строго индивидуально и варьируют от 10—15 мг в сутки при хрон, заболеваниях до 100—200 мг при неотложных состояниях (шоке, иммунол. конфликтах и др.); курсовые дозы аналогично колеблются (3—4 г, иногда выше). При острых заболеваниях возможно применение максимально допустимых доз (для ликвидации иммунол, конфликта). При приеме внутрь действие препарата проявляется быстрее, но продолжается не более 6—8 час.; при внутримышечном введении действие из-за медленного всасывания проявляется несколько позднее, зато продолжается 8—12 час.
Противопоказания: сахарный диабет, тяжелая форма артериальной гипертензии (гипертоническая болезнь, заболевания почек), язвенная болезнь, остеопороз, беременность.
Форма выпуска ацетата кортизона: порошок, таблетки по 0,025 г и 0,05 г; суспензии для внутримышечных инъекций (по 0,025 г в 1 мл) во флаконах по 10 мл. Сохраняют в прохладном и защищенном от света месте, в склянках темного стекла; список Б.
См. также Кортикостероиды, препараты.
Библиография: См. библиогр, к ст. Кортикостероиды.
А. И.Воробьев, Ю. Л.Милевская.
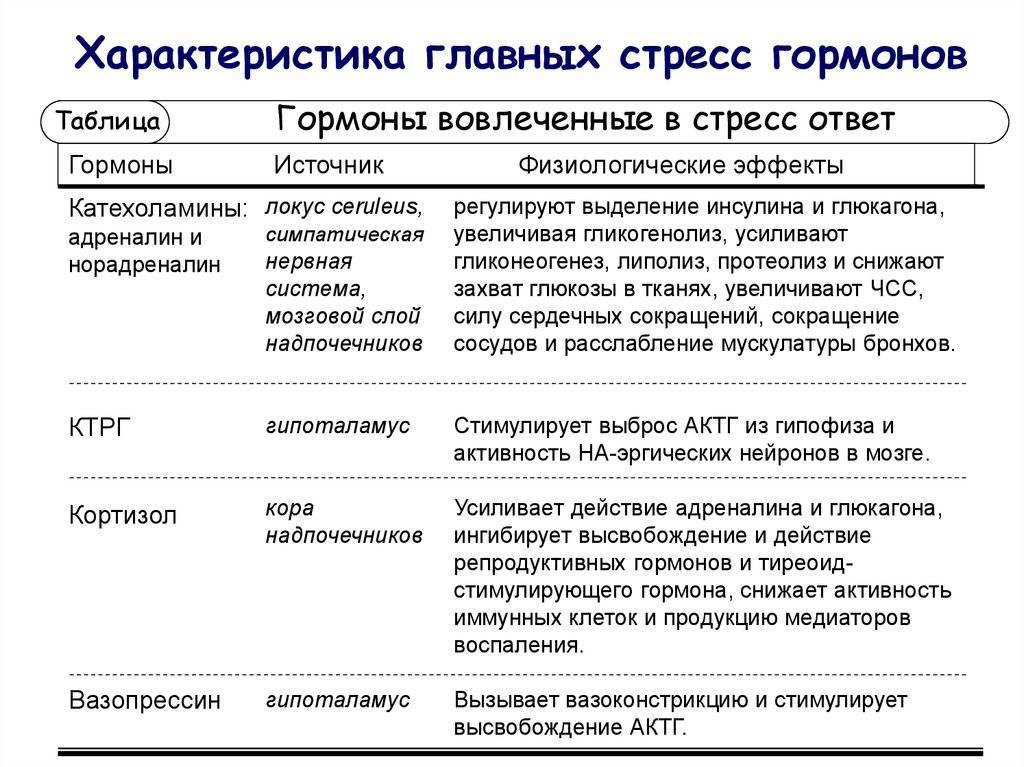
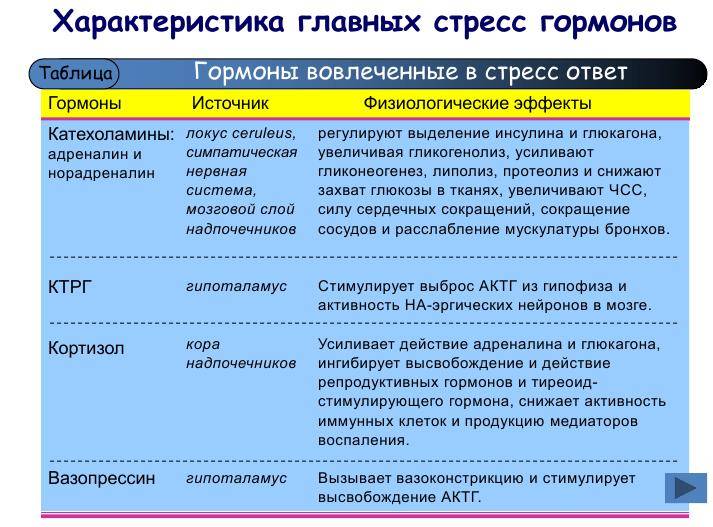
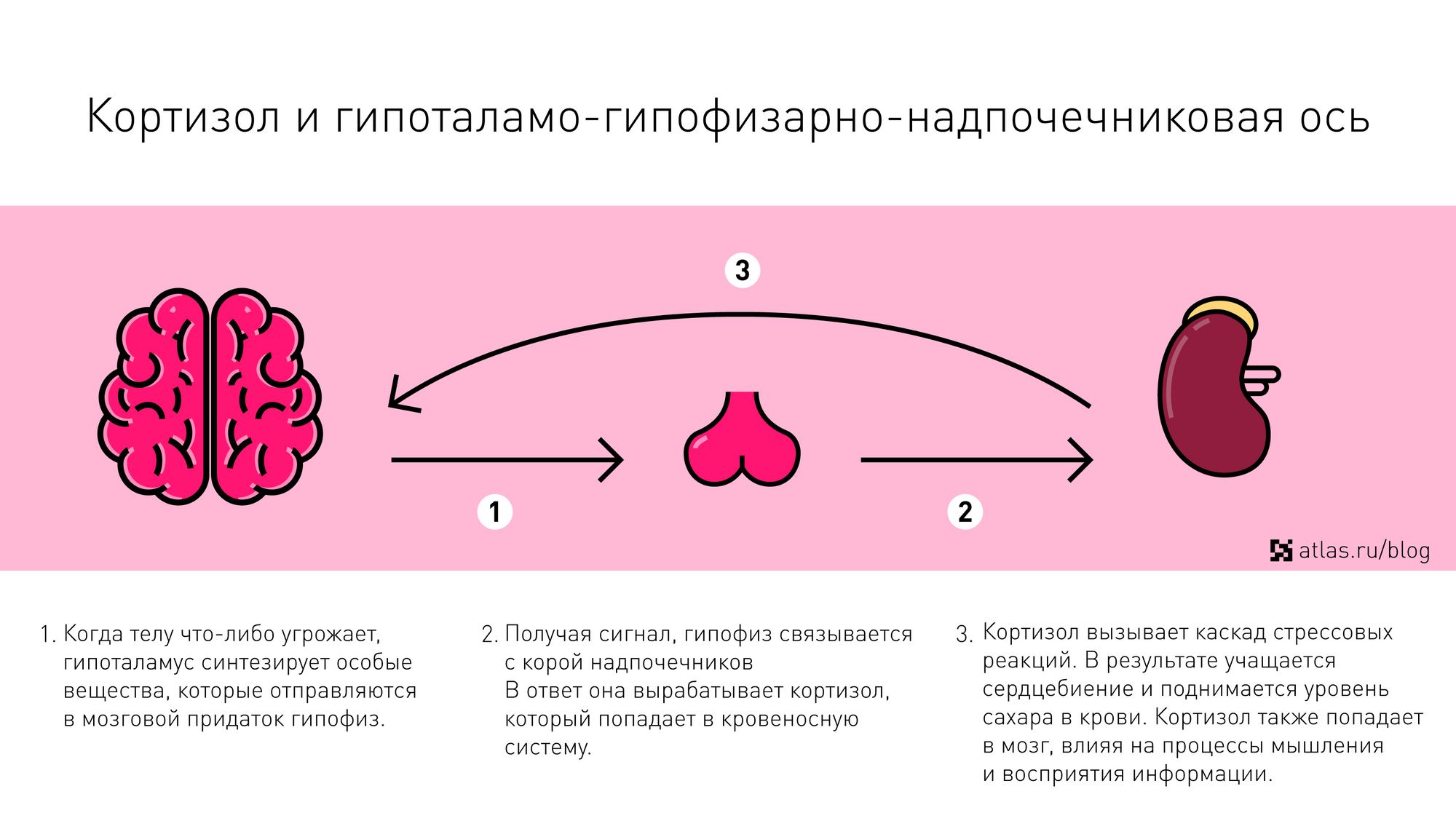
Что же это такое – «стрессовый» гормон кортизол?
Кортизол – главный в группе глюкокортикоидов, которые постоянно циркулируют по кровеносному руслу. Связываясь с белками (альбумин, кортикостероид-связывающий глобулин – транскортин), он забирает на себя львиную долю (до 90%) всех гормонов, синтезируемых корой надпочечников. Некоторое количество (приблизительно 10%) в виде биологически активной фракции присутствует в плазме само по себе, не соединяясь с протеинами, это – свободный кортизол, который не будет испытывать каких-либо обменных превращений и в дальнейшем (после фильтрации в клубочках почек) удалится из организма.
В кровеносном русле кортизол передвигается, будучи соединенным с белком-носителем – кортикостероид-связывающим глобулином. Протеин, переносящий 17-гидрокортикостерон, производится клетками печени и, помимо транспортной функции, выступает в роли резервуара данного гормона в крови. Белок-носитель, связавшись с кортизолом, транспортирует его к клеткам-мишеням. Попав в печень, гормон претерпевает различные превращения, в результате которых образуются водорастворимые метаболиты, не обладающие какой-либо гормональной активностью. Впоследствии они покинут организм с помощью выделительной системы (через почки).
Биологическая роль кортизола чрезвычайно высока. Этот гормон принимает активное участие в различных процессах метаболизма, однако особые отношения у него сложились с обменом углеводов. Кортизол активизирует глюконеогенез – образование глюкозы из других веществ, которые не содержат углеводов, но могут обладать энергетическим ресурсом: пировиноградная кислота (пируват), свободные аминокислоты, молочная кислота (лактат), глицерол.
Регулируя углеводный обмен, кортизол помогает организму пережить голодание, не позволяет глюкозе опуститься ниже критической отметки (форсирует синтез сахаров и тормозит их распад). Кортизол – важный защитник организма от любого нарушения физиологического баланса, то есть, от стресса, за что ему дали название – «стрессовый» гормон.
Вот основные действия, которые производит кортизол в организме:
- Оказывает влияние на белковый обмен, снижая продукцию протеинов в клетках, усиливает процессы катаболизма;
- Влияет на уровень концентрации таких значимых макроэлементов, как натрий (Na) и кальций (Ca);
- Уменьшая потребление клетками сахара, увеличивает его количество в крови (поэтому повышение гормона способствует развитию стероидного диабета);
- Помогает расщеплять жиры, увеличивает уровень свободных жирных кислот, усиливая их мобилизацию, и, таким образом, помогает обеспечению организма энергией;
- Участвует в регуляции кровяного давления;
- Несет противовоспалительный эффект за счет стабилизации мембран клеточных органоидов (лизосом), снижения проницаемости сосудистых стенок, участия в иммунологических реакциях.
Синдром Кушинга: прогноз излечения
После операции пациент должен проходить регулярные осмотры. Врач будет проверять успешность проведения операции на основе анализа крови. Это необходимо для выявления рецидивов на ранней стадии.
Эндокринолог проверяет, нужно ли увеличить или уменьшить дозу кортизола, поскольку кортизол – важный стрессовый гормон в организме. В некоторых ситуациях организму требуется больше кортизола – при лихорадочных заболеваниях, операциях или других стрессовых ситуациях дозу кортизола необходимо увеличить.
Если у пациента на одном надпочечнике есть опухоль, вырабатывающая кортизол, то кора второго надпочечника обычно значительно снижает выработку этого гормона. После удаления опухоли здоровому надпочечнику нужно время, чтобы восстановиться. Поэтому этим пациентам приходится принимать кортизол в течение 2 лет и более после операции.
Высокий кортизол и низкий уровень гормона
Высокий кортизол в крови, вернее, увеличение его содержания, наблюдается в ряде патологических состояний. Безусловно, главными причинами подобных расстройств (повышение гормона в крови и моче), считаются заболевания эндокринной системы, вместе с тем, нельзя утверждать, что другие болезни и даже физиологические состояния не способны повлиять на уровень кортизола, попав в те или иные ситуации. Например, кортизол повышен в случаях:
- Болезни (избыточный синтез АКТГ) и синдрома Иценко-Кушинга (поражение надпочечников – чрезмерная выработка гормона);
- Опухоли надпочечников;
- Значительного влияния стресса, что, как правило, наблюдается у людей, страдающих другой тяжелой патологией;
- Острых психических расстройств;
- Инфекционного процесса в остром периоде;
- Отдельных злокачественных опухолей (выделение кортизола эндокринными клетками, расположенными в других органах – поджелудочная железа, тимус, легкие);
- Некомпенсированного сахарного диабета;
- Терапии препаратами некоторых фармацевтических групп и, в первую очередь, эстрогенами, кортикостероидами, амфетамином;
- Терминальных состояний (по причине нарушения процессов диссимиляции кортизола);
- Астматического статуса;
- Шоковых состояний;
- Серьезного поражения печеночной и почечной паренхимы;
- Острого алкогольного опьянения у людей, не склонных к злоупотреблению;
- Постоянного поступления никотина в организм (у курильщиков со стажем);
- Ожирения;
- Повышенной эмоциональной возбудимости (даже при венепункции);
- Длительного использования оральных контрацептивов;
- Беременности.
Постоянное повышение уровня кортизола в силу любых обстоятельств, пусть даже не связанных с серьезными нарушениями функции надпочечников, может оказывать негативное влияние на весь организм:
- Страдает нервная система, а в результате этого падают интеллектуальные способности;
- Расстраивается деятельность щитовидной железы;
- Повышается артериальное давление, нередко приводящее к гипертоническим кризам;
- Появляется чрезмерный аппетит, что приводит к увеличению массы тела;
- У женщин начинаются проблемы в виде гирсутизма (мужской тип оволосения), изменения фигуры по кушингоидному типу;
- По ночам одолевает бессонница;
- Снижается защита организма от различного рода инфекционных агентов;
- Увеличивается риск развития инфарктов и инсультов.
Перечисленные выше симптомы не могут не насторожить человека, оставив его равнодушным к своему здоровью, ведь они, заметно влияя на жизненную активность, омрачают саму жизнь.
Низкий кортизол или снижение его концентрации в крови также имеет свои причины, это:
- Первичная недостаточность надпочечников (например, болезнь Аддисона в результате апоплексии, кровоизлияния);
- Функциональная несостоятельность гипофиза;
- Дефицит гормонов щитовидной железы, который влечет уменьшение количества кортизола;
- Длительное использование в качестве лечения адренокортикотропного гормона или глюкокортикоидов (торможение функциональных способностей коры надпочечников);
- Недостаток отдельных ферментов, в частности, 21-гидроксилазы, без которых синтез данного гормона затруднен;
- Неспецифический инфекционный полиартрит, остеоартрит, ревматоидный артрит, спондилит;
- Бронхиальная астма;
- Хронический гепатит, цирроз;
- Применение некоторых медикаментозных средств: даназол, леводопа, трилостан, морфин и др.
- Подагра.
Низкий кортизол в крови может быть следствием такой тяжелой патологии, как гипокортицизм или болезнь Аддисона, развивающаяся по разным причинам. Недостаточная продукция гормона в данном случае обусловлена патологией самих надпочечников, которые не могут синтезировать нужное организму количество глюкокортикоидов, в том числе, и кортизола. Гипокортицизм дает симптомы, которые трудно не заметить: хроническая усталость, слабость мышечного аппарата, расстройство пищеварения, бронзовая окраска кожи (болезнь Аддисона поэтому называют еще бронзовой болезнью), дрожание конечностей, учащенное сердцебиение, уменьшение объема циркулирующей крови (ОЦК) за счет обезвоживания.
Анализ на кортизол
Безусловно, если в лаборатории предстоит определить гормон стресса, то для получения достоверных результатов, подход к анализу на кортизол, должен быть соответствующим. Простое, на первый взгляд, волнение может запросто исказить результаты, и пациенту придется сдавать кровь повторно (или введет в заблуждение врача?), ведь нет сомнения в том, что кортизол в этом случае будет повышен.
Человеку, которому назначено данное исследование, сначала объясняют значимость анализа (он позволит узнать связаны ли клинические проявления болезни с гормональным сдвигом либо причина симптомов кроется в чем-то другом). Пациент заранее знает, в какое время нужно сдать анализ, а также, что кровь будет взята из вены (у некоторых даже от наложения жгута можно ждать повышения кортизола)
Затем больному предлагают обратить внимание на несколько важных пунктов, которые он обязан выполнить перед тем, как у него возьмут кровь:
- За 3-е суток до исследования начинает контролировать содержание поваренной соли в своем рационе, оно не должно превышать 3 г в сутки;
- За 2-е суток прекращает прием фармацевтических средств, способных повлиять на значения кортизола в крови (андрогены, эстрогены и др.), но если лекарства применяются по жизненным показаниям и отмена невозможна, то в бланке анализа обязательно должна быть отметка;
- Пациент приходит в лабораторию натощак, воздержавшись от еды не менее 10 часов (10 – 12), а также ограничив физическую активность (10 – 12 часов);
- За полчаса до анализа человек, сдающий кровь на кортизол, должен прилечь и максимально расслабиться.
Наиболее достоверные результаты получаются, если отбор образцов крови на исследование производится в интервале 6 – 9 часов утра.
пример динамики кортизола в течение суток, наивысший уровень – в течение часа после подъема
Кортизол и метаболический синдром
Хорошо известно, что ГКС оказывают влияние на распределение жировой ткани. Ряд исследований показал, что пациенты с ожирением имеют гиперактивацию фермента 11β-HSD1 в жировой ткани и гепатоцитах, ключевого фермента, стимулирующего конверсию метаболически неактивного кортизона в активный кортизол (рис. 1). Напротив, 11β-гидроксистероид дегидрогеназа 2 (11β-HSD2), катализирующая превращение кортизона в кортизол, имела низкую экспрессию.
Рис.1 Конверсия кортизола в кортизон
Как упоминалось ранее, было выдвинуто предположение, что активность 11β-HSD1 может быть одним из патогенетических механизмов, лежащих в основе развития метаболического синдрома. Данные экспериментальных исследований на животных показали, что селективная 11β-HSD1 гиперэкспрессия в жировой ткани (аналогично тому, что наблюдается у пациентов с ожирением) приводила к развитию метаболического синдрома, и, в частности, дислипидемии, ожирению, гипертензии, связанной с активацией системы ренин-ангиотензин-альдостерон, инсулинорезистентности и нарушению углеводного обмена. Кроме того, адипоциты имели больший размер (рис. 2), чем обычно, основной эффект наблюдался в висцеральной жировой ткани, возможно, из-за более высокой плотности рецепторов к ГКС .
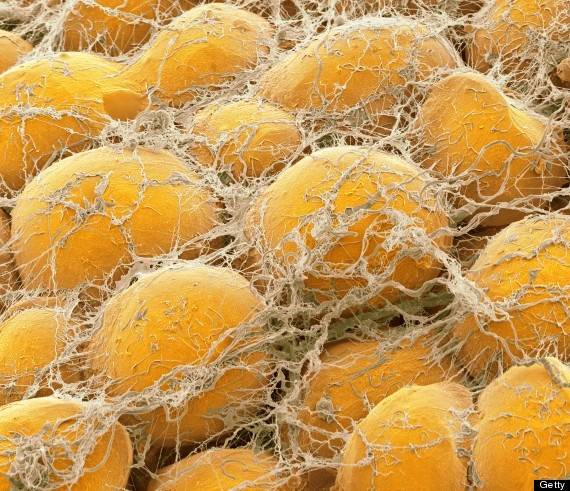
Рис. 2 Электронная микрофотография адипоцитов
Полученные данные позволили рассматривать 11b-HSD1 в качестве новой мишени для фармакотерапии. II фаза рандомизированного двойного слепого плацебо-контролируемого исследования эффективности селективного ингибитора 11b-HSD1 (INCB013739) у пациентов с избыточной массой тела/ожирением и СД 2 типа показали статистически значимое увеличение печеночной и периферической чувствительности к инсулину, снижению глюкозы в плазме натощак, общего холестерина и липопротеинов низкой плотности (ЛПНП), триглицеридов плазмы и уровня АД . Открытым остается вопрос: каким образом локальная гиперпродукция ГКС влияет на системный уровень кортизола и нарушается ли при этом механизм отрицательной обратной связи?
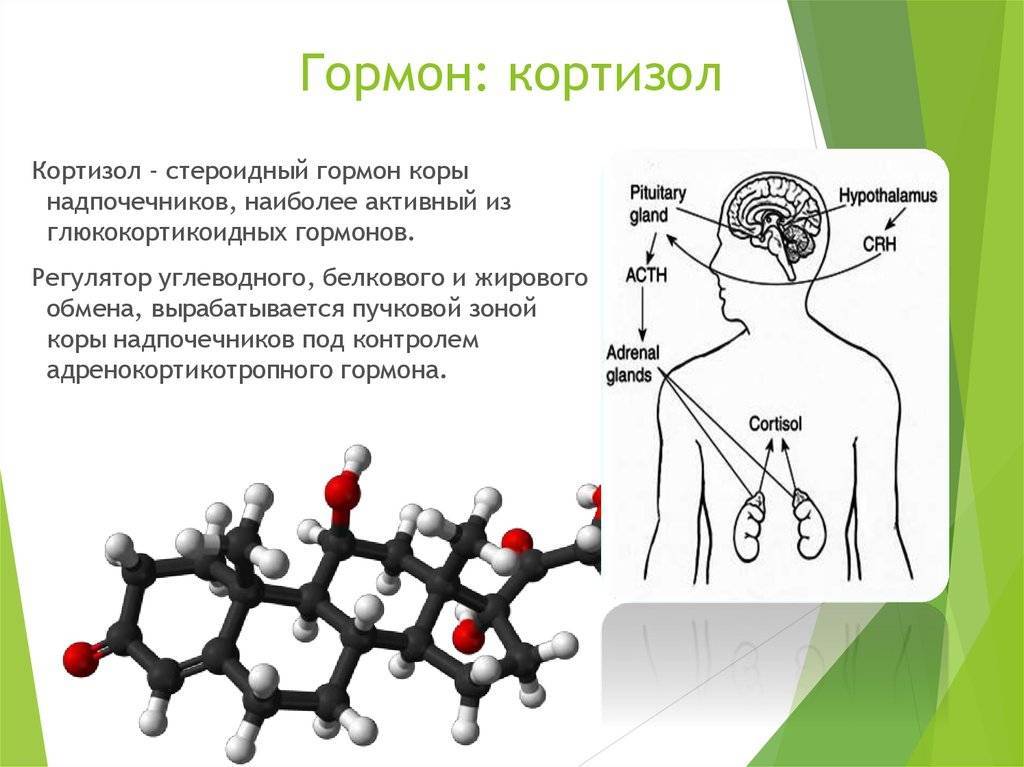
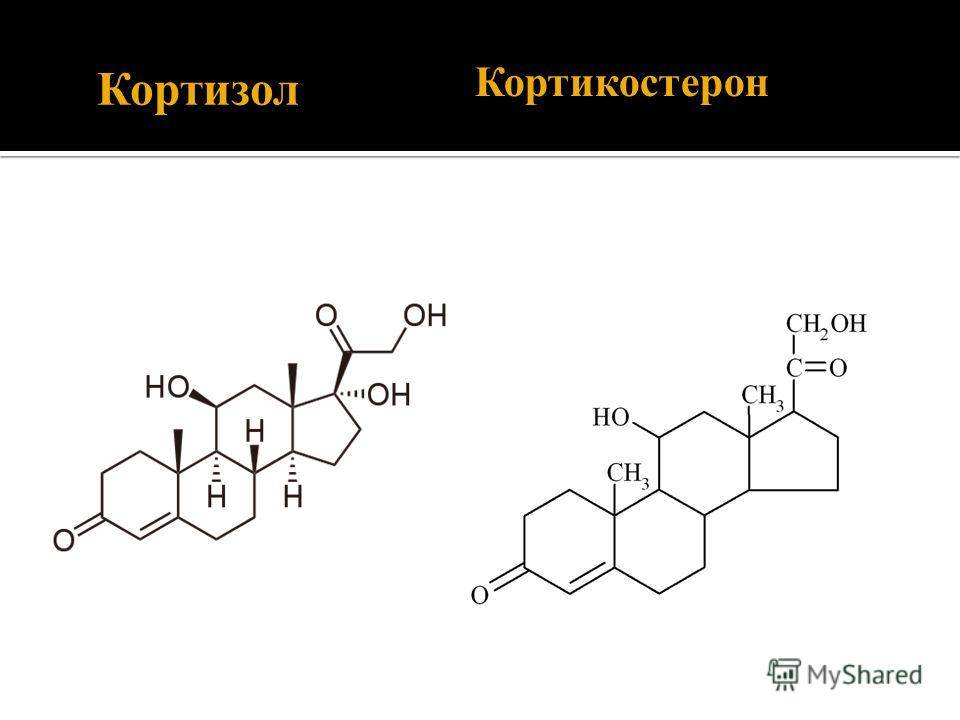
Кортизол
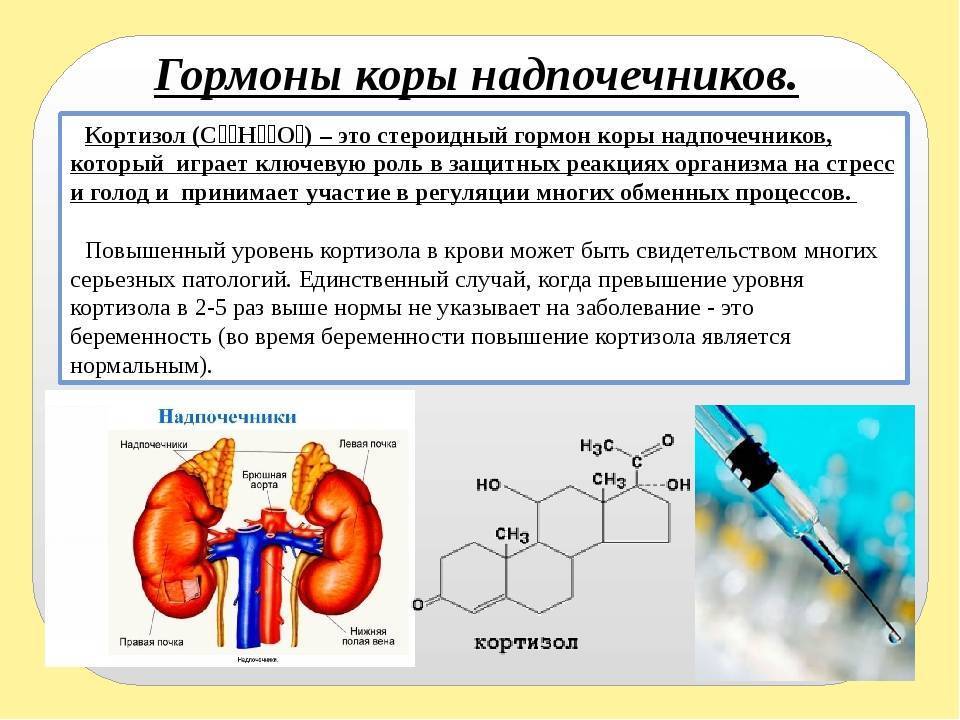
Общая характеристика
Кортизол выделяется корой надпочечников под воздействием адренокортикотропного гормона (АКТГ). Химическая природа кортизола – стероид, что означает, что он легко проникает в клетки. Органами-мишенями являются большинство клеток организма человека.
Секреция кортизола
Пик деятельности надпочечников приходится на утренние часы: от 6 до 8 часов. В это время фиксируются максимальные значения секреции кортизола. В первые минуты после пробуждения содержание кортизола быстро нарастает. Прирост составляет 50–100% по сравнению с уровнем в начале бодрствования. Затем концентрация гормона начинает снижаться, но у проснувшихся рано, снижение секреции кортизола происходит медленнее. После 20 часов концентрация кортизола минимальна (рис. 1).
Рис. 1. Изменение секреции кортизола в течение дня
Концентрация кортизола
В норме концентрация кортизола в крови составляет 150-770 нмоль/л (10% свободного кортизола и 90% «связанного»). Хроническое превышение нормальных значений уровня кортизола может вызвать иммунные и онкологические заболевания. От пола и возраста уровень кортизола практически не зависит.
Функции кортизола
Кортизол поддерживает гомеостаз глюкозы, вызывая глюконеогенез, который сопровождается катаболизмом белков, стимулирует распад жира в одних частях тела и запасание жира в других, оказывает противовоспалительное действие и подавляет иммунитет, способствует развитию остеопороза.
Влияние силовой тренировки на концентрацию кортизола в крови
Показано, что сразу после выполнения силовых упражнений концентрации АКТГ и кортизола в крови значительно возрастают. Программы силовой тренировки, вызывающие максимальное повышение концентрации кортизола и лактата в крови человека, характеризует большой объём работы, интенсивность (величина отягощения) от среднего до высокого уровня и короткие периоды отдыха между сетами.
Влияние аэробной тренировки на уровень кортизола в крови
Интенсивность (мощность) аэробной тренировки значительно влияет на секрецию кортизола. Если интенсивность превышает 60% МПК концентрация кортизола в крови возрастает. Это стандартный ответ организма человека на нагрузку. Высокий фоновый уровень кортизола в крови может приводить к уменьшению концентрации этого гормона при выполнении аэробных упражнений с интенсивностью более 60% МПК.
Состояние перетренированности
Увеличение объёма силовой работы в состоянии перетренированности сопровождается снижением в состоянии покоя концентрации в крови тестостерона, инсулина и повышением концентрации кортизола. Индекс анаболизма снижается.
Литература
- Эндокринная система, спорт и двигательная активность. – Киев: Олимпийская литература, 2008. – 600 с.
- Самсонова А.В. Гормоны и гипертрофия скелетных мышц человека: учеб. пособие. – СПб: Кинетика, 2019.– 204 с.
Синтез кортизола в коже. Регуляция репарации
Ожирение и ассоциированные с ожирением состояния сопровождаются нарушениями физиологической репарации, что увеличивает вероятность замедленного заживления ран. Люди с ожирением имеют высокий риск развития венозных язв, различных кожных заболеваний (например, кандидоза, эритразмы) или более серьезных кожных инфекций (например, целлюлита, некротизирующего фасцита), гнойных осложнений после хирургических вмешательств. Однако роль ГКС в регуляции репарации ран в настоящее время достаточно плохо изучена.
Наряду с тканью надпочечников, синтезирующей глюкокортикоиды, все больше данных стало появляться о местах вненадпочечниковой продукции кортизола, к ним относятся мозг, легкие, сердце, тимус, клети иммунной системы и кожа .
Несмотря на основную функцию кожи служить барьером для защиты внутренней среды организма от агрессивных воздействий, последние исследования в дерматологии были посвящены изучению способности клеток эпидермиса секретировать гормоны. Способность взаимодействовать с центральной нервной системой посредством локальной продукции в системный кровоток гормонов, нейропептидов, нейротрансмиттеров и других регуляторных факторов позволяет рассматривать кожу как нейроэндокринный орган .
Кератиноциты – первые клетки, которые реагируют на повреждение целостности кожного покрова, запускающего каскад реакций, что способствует изменению фенотипа кератиноцитов, приводит к их миграции и пролиферации, изменению способности кератиноцитов к адгезии и конфигурации цитоскелета (рис. 3).
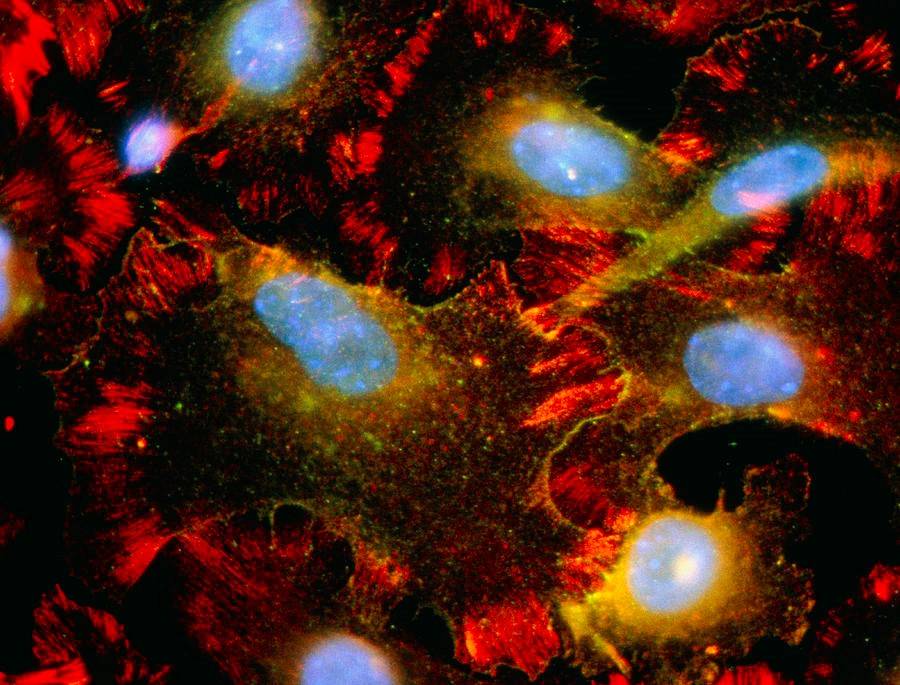
Рис. 3 Иммунофлюоресцентная микрофотография кератиноцитов
Кератиноциты обладают способностью синтезировать холестерин, который является предшественником всех стероидных гормонов. Кроме того, как показывает ряд исследований, клетки кожи способны секретировать гипоталамо-гипофизарные гормоны: проопиомеланокортин, адренокортикотропный гормон, тиреотропный гормон и соматотропный гормон .
Экспрессия ключевых ферментов стероидогенеза в коже подтверждает предположение о том, что эпидермис может быть основным местом вненадпочечникового синтеза кортизола. Как и ожидалось, ферменты, которые контролируют активность кортизола, а именно конверсию в неактивный кортизон 11b-HSD1 и 11b-HSD2, также экспрессируются множеством подтипов кератиноцитов. Экспрессия CYP11B1 преимущественно выражена в базальных и супрабазальных слоях эпидермиса. Эти слои эпидермиса имеют наибольшую способность к пролиферации и являются основными источниками для регенерации тканей .
Экспрессия CYP11B1, ключевого фермента синтеза кортизола, повышается в ответ на воздействие АКТГ или провоспалительных цитокинов IL-1, что свидетельствует о прямом стимулирующем действии провоспалительных цитокинов и снижается в ответ на метирапон. По всей видимости, секреция кортизола в ответ на повреждение ткани сначала повышается и достигает пика спустя 48 ч после воздействия повреждающего агента, а затем, при переходе раны в стадию пролиферации, постепенно снижается к исходному уровню спустя 96 ч, что подтверждают данные исследований на культуре человеческих кератиноцитов. Спустя 96 ч увеличивается экспрессия 11-HSD2 – фермента, конвертирующего преобразование активного кортизола в неактивный кортизон. Чтобы подтвердить предположение о существовании отрицательной обратной связи кортизол/IL-1, в культуру клеток добавляли ингибитор синтеза кортизола – метирапон. По сравнению с контролем, в группе метирапона отмечалось повышение экспрессии IL-1, что подтверждает наличие петли обратной связи, которая регулирует первоначальный ответ на повреждение ткани, предотвращая избыточное воспаление, которое может привести к дальнейшему повреждению тканей.
По данным последних исследований, глюкортикоиды действуют через Wnt-сигнальный путь, тем самым влияя на клеточный цикл кератиноцитов, ингибируя пролиферацию, миграцию, и индуцируя клеточную дифференцировку. Кроме того, ГКС ингибируют влияние эпидермального фактора роста (EGF), который непосредственно стимулирует миграцию и пролиферацию клеток .
Таким образом, даже при функциональном гиперкортицизме за счет описанных механизмов нарушается нормальная репарация ткани. Эпидермис ран теряет способность к пролиферации и миграции, что может приводить к длительной персистенции раневых де фектов.
Как врачи находят причину синдрома Кушинга?
Если врач-эндокринолог диагностирует синдром Кушинга, то назначаются дополнительные исследования и анализы. Они помогают определить источник проблемы – гипофиз, эктопия или надпочечники
Знание источника важно при выборе наилучшего типа лечения
Анализы крови
Первый шаг – измерение уровня АКТГ в крови. Если уровни АКТГ низкие, то вероятная причина – опухоль надпочечников. Людям с опухолями надпочечников дополнительные анализы крови не нужны.
Если уровень АКТГ нормальный или высокий, то вероятная причина – опухоль гипофиза или эктопическая опухоль.
Другие анализы крови помогают отличить опухоли гипофиза от эктопических опухолей. Эндокринолог обычно назначает следующие анализы:
- Тест стимуляции кортиколиберином. Для этого анализа пациенту сделают укол CRH. Если у него опухоль гипофиза, КРГ повысит уровень АКТГ и кортизола в крови. Это редко случается у людей с эктопическими опухолями.
- Супрессивный тест с высокими дозами дексаметазона – HDDST. Этот тест аналогичен LDDST, за исключением того, что в нем используются более высокие дозы дексаметазона. Если уровень кортизола в крови падает после приема высокой дозы дексаметазона, у пациента, вероятно, опухоль гипофиза. Если уровень кортизола не снижается, то возможна опухоль в другой части тела.
Другие исследования
Другие исследования ищут опухоли и помогают отличить опухоли гипофиза от эктопических опухолей.
Процедуры визуализации — УЗИ, КТ, МРТ при синдроме Кушинга
Если лабораторные тесты выявили опухоль как причину повышенного уровня кортизола, ее исследуют более тщательно с использованием соответствующих методов визуализации:
- Опухоль в коре надпочечников диагностируют с помощью УЗИ, компьютерной томографии или магнитно-резонансной томографии брюшной полости;
- При наличии опухоли в гипофизе исследование проводят с помощью магнитно-резонансной томографии;
- Если в гипофизе нет опухоли, врач ищет ее в другом органе, с помощью УЗИ, КТ или МРТ.
Визуализирующие тесты показывают размер и форму гипофиза и надпочечников и ищут опухоли, помогают определить их местонахождение.
Анализ крови из каменистого синуса
Опухоли гипофиза обычно небольшие и могут не обнаруживаться при визуализации. Если МРТ не показывает опухоль гипофиза, то проводится анализ крови из каменистого синуса. Этот тест – лучший способ отличить опухоль гипофиза от эктопических причин синдрома Кушинга.
Врач возьмет образцы крови из каменистых синусов — вен, дренирующих гипофиз. В то же время берется образец крови из кровеносного сосуда, находящегося далеко от гипофиза.
Более высокие уровни АКТГ в крови из каменистых синусов, чем из других кровеносных сосудов, указывают на опухоль гипофиза. Сходные уровни АКТГ во всех образцах крови свидетельствуют об эктопической опухоли.
Источники
- Bulska M., Szczesniak P., Pieta-Dolinska A., Dorobek P., Parafiniuk J., Oszukowski P., Orszulak-Michalak D. Different modes of delivery and hormonal stress response. // Ginekol Pol – 2021 – Vol – NNULL – p.; PMID:33844248
- Chantzichristos D., Svensson PA., Garner T., Glad CA., Walker BR., Bergthorsdottir R., Ragnarsson O., Trimpou P., Stimson RH., Borresen SW., Feldt-Rasmussen U., Jansson PA., Skrtic S., Stevens A., Johannsson G. Identification of human glucocorticoid response markers using integrated multi-omic analysis from a randomized crossover trial. // Elife – 2021 – Vol10 – NNULL – p.; PMID:33821793
- Yan D., Zhang X., Chen C., Jiang D., Liu X., Zhou Y., Huang C., Zhou Y., Guan Z., Ding C., Chen L., Lan L., Fu X., Wu J., Li L., Yang S. Characteristics of Viral Shedding Time in SARS-CoV-2 Infections: A Systematic Review and Meta-Analysis. // Front Public Health – 2021 – Vol9 – NNULL – p.652842; PMID:33816427
- Lai CH., Ho SC., Pan CH., Chen WL., Wang CC., Liang CW., Chien CY., Riediker M., Chuang KJ., Chuang HC. Chronic exposure to metal fume PM2.5 on inflammation and stress hormone cortisol in shipyard workers: A repeat measurement study. // Ecotoxicol Environ Saf – 2021 – Vol215 – NNULL – p.112144; PMID:33743405
- Ishii M., Horita N., Takeuchi M., Matsumoto H., Ebina-Shibuya R., Hara Y., Kobayashi N., Mizuki N., Kaneko T. Inhaled Corticosteroid and Secondary Glaucoma: A Meta-analysis of 18 Studies. // Allergy Asthma Immunol Res – 2021 – Vol13 – N3 – p.435-449; PMID:33733638
- Rosa IN., de Sousa Munhoz Soares AA., Rodrigues MP., Naves LA. Classic cardiovascular risk factors improve in very elderly hypopituitary patients treated on standard hormone replacement in long term follow- up. // Clin Diabetes Endocrinol – 2021 – Vol7 – N1 – p.6; PMID:33731193
- Liu L., Jing FY., Wang XW., Li LJ., Zhou RQ., Zhang C., Wu QC. Effects of corticosteroids on new-onset atrial fibrillation after cardiac surgery: A meta-analysis of randomized controlled trials. // Medicine (Baltimore) – 2021 – Vol100 – N11 – p.e25130; PMID:33725992
- Pinna SM., Scabini S., Corcione S., Lupia T., De Rosa FG. COVID-19 pneumonia: do not leave the corticosteroids behind! // Future Microbiol – 2021 – Vol16 – NNULL – p.317-322; PMID:33709775
- Juul S., Nielsen EE., Feinberg J., Siddiqui F., Jørgensen CK., Barot E., Holgersson J., Nielsen N., Bentzer P., Veroniki AA., Thabane L., Bu F., Klingenberg S., Gluud C., Jakobsen JC. Interventions for treatment of COVID-19: Second edition of a living systematic review with meta-analyses and trial sequential analyses (The LIVING Project). // PLoS One – 2021 – Vol16 – N3 – p.e0248132; PMID:33705495
- Chalmers JD., Crichton ML., Goeminne PC., Cao B., Humbert M., Shteinberg M., Antoniou KM., Ulrik CS., Parks H., Wang C., Vandendriessche T., Qu J., Stolz D., Brightling C., Welte T., Aliberti S., Simonds AK., Tonia T., Roche N. Management of hospitalised adults with coronavirus disease 2019 (COVID-19): a European Respiratory Society living guideline. // Eur Respir J – 2021 – Vol57 – N4 – p.; PMID:33692120








![Анализ крови на кортизол [сдать, подготовка и расшифровка]](https://roliki-magazin.ru/wp-content/uploads/0/7/2/07208aae14826445db74adf2281b951c.jpeg)